体外释放(IVRT)
评估外用制剂的药物释放率和程度,是质量研究及稳定性考察中的重要指标。
指导处方工艺开发及优化。
体外透皮(IVPT)
模拟外用制剂在生理条件下的经皮渗透过程,为评价制剂的安全性和有效性提供参考和保证。
建立体内和体外相关性,指导临床研究。
新药加速
针对创新药研发,可快速筛选合适处方,加速新药研究过程。
研究内容 | 体外释放(IVRT) | 体外透皮(IVPT) |
参考法规 | CDE、FDA、EMA、ICH M10、ChP9012 | CDE、FDA、EMA、ICH M10、ChP9012 |
方法开发 | 制备方法:设备确认、接收介质、合成膜、取样时间点、上样量、介质体积等筛选 分析方法:专属性、定量范围 | 制备方法:设备确认、皮肤(中国:离体巴马小香猪皮、美国:离体人皮)、接收介质、取样时间点、给药剂量和给药方式、方法灵敏度、质量平衡 分析方法:专属性、定量范围 |
分析方法验证 | 标准曲线、选择性、基质效应、残留、灵敏度、 准确度与精密度、稀释可靠性、稳定性 | 标准曲线、选择性、基质效应、残留、灵敏度、准确度与精密度、稀释可靠性、稳定性 |
制备方法验证 | 设备性能确认、膜表面温度、取样泵性能、膜确认、接收介质确认、取样确认、精密度与重现性、线性与范围、剂量消耗、区分力、耐用性、环境控制等 | 设备性能确认、皮肤表面温度、皮肤确认、接收介质确认、取样确认、渗透曲线与范围、精密度与重现性、剂量消耗、区分力、环境控制等 |
评价标准 | FDA: ·累积释放量与 t1/2 呈线性(r2≥0.97) ·90%置信区间在75~133.33%的限度范围 ·每批样品所得的释放速率 K 的 RSD≤15% EMA:90%置信区间在90~111%的限度范围 CDE:视具体品种确定 | ·等效性参数(Jmax和Atotal)试验样品与参比制剂均值之比的可接受标准:90%置信区:80.00%~125.00% ·物料平衡(回收率):90~110% ·皮肤滞留量(药物在皮肤中的分配)单独分析(视品种而定) ·时滞相同(±10%)(如有需要) |
难
皮肤差异大
动物皮在厚度、结构、通透性等方面有显著差异,而该差异会严重影响实验结果的稳定性与重现性,从而使等效性评价的样本量显著增加,导致研究成本大幅增加甚至可能造成结果无法等效。
解
稳定的皮肤来源+熟练制备技术
我们有成熟稳定的动物皮供应商,通过严格把控动物皮的种属、来源、部位,运用熟练的皮肤制备技术,可显著降低等效性评价的样本量,从而有效降低研究成本。
难
药物渗透难
因动物皮的多层次结构,亲水性或亲脂性、大分子药物很难通过,尤其是低剂量制剂,透皮愈加困难,进而导致无法进行透皮行为评价。
解
建立促渗剂库
我们在不改变皮肤屏障的作用下,筛选并建立了对皮肤亲和的促渗剂库,可以根据产品特性,快速、有效解决药物渗透难题。
外用制剂
为外用制剂产品质量、安全及疗效保驾护航。
医疗器械
确保伤口敷料、植入式给药装置等产品疗效显著且安全可靠。
化妆品
助力化妆品功效宣称,提供坚实有力的专业技术支撑力。
100+
研究品种超100(创新药约占40%、发补约占10%)
剂型多样
软膏、乳膏、凝胶、乳胶、纳米混悬液、涂膜剂、搽剂、泡沫剂等
设备高端
Logan 透皮仪,Delfin 经皮水分测定仪,LCMS,冰冻切片机,显微共聚焦拉曼等
体系完善
基于 FDA、EMA、CDE 等指导原则,建立完善高效评价流程
服务灵活
可根据客户的需求定制方案(优效/等效评价等)
实力雄厚
中美双报经验丰富,项目管理科学高效,研究全面发补少
品种 | 工作内容 | 类别 | 难点 |
ITR2202 | 通过 IVRT、IVPT 进行新药处方筛选和质量研究 | 临床 I 期 | ·疏水性药物介质筛选 ·API 容易降解 |
ITR2303 | 通过 IVRT、IVPT 进行新药处方筛选和质量研究 | 临床 I 期 | ·本品为乳胶剂型 ·上样方式、上样量、按摩、人工膜、漏槽介质等参数需要系统研究 |
ITR2302 | 通过 IVRT、IVPT 进行新药处方筛选和质量研究 | 临床前研究 | ·本品为纳米混悬液复杂制剂 ·上样方式、上样量、按摩、人工膜、漏槽介质等参数需要系统研究 |
CD2401 | 通过 IVRT、IVPT 进行新药处方筛选 | 临床前研究 | ·疏水性药物介质筛选 ·分子经皮吸收量极低 |
低剂量激素软膏剂 | IVRT、IVPT 请增加不同粒径 API 的研究,已证明方法均有合适的区分性 | 发补研究 | ·方法区分性的评价 |
表面麻醉制剂 | 关注各国药典要求,进行 IVRT、IVPT研究 | 发补研究 | ·各国药典方法开发和验证要求的确认,评估符合性 ·样本量和猪皮复合性要求 |
某维A酸类外用制剂 | 参考 EMA 指导原则,计算相关的渗透参数—最大吸收速率(Jmax)和在实验结束时单位面积渗透的总量(Atotal),比较自制制剂和参比制剂平均值比率的90%置信区间,关注样本量,并对皮下透过量、皮上药物残留量、皮内药物滞留量及上述3个数据的回收率进行比较 | 发补研究 | ·疏水性药物介质筛选 ·透过量极低或者不透药物皮内、皮下、药物滞留评价 ·样本量要求 |
PDE-4抑制剂外用制剂 | IVRT、IVPT 开发、验证 | 零发补 | ·上样方式的选择 ·剂量维持时间的选择 |
某固定剂量复方制剂 | IVRT、IVPT 开发、验证 | 在研项目 | ·处方占比极低,释放和透过量极低 ·复方两 API 释放趋势不一致,需筛选合适的方法,并指导处方工艺开发 |
CDE常见的缺陷项
接受介质筛选的合理性
动物皮来源、部位及选择标准、皮肤管理 SOP 等
方法区分性补充验证(比如:混选型制剂,不同粒径区分性实验)
IVPT:关注各国法规研究要求,注重样本量分析,等效性评价的要求等
需提供完善的方法学研究(特别是针对不透皮的药物:皮上药物量、皮内药物残留和皮下药物透过量)
案例分析
1
案例
通过 IVRT 和 IVPT 研究不同处方的释放和皮肤药代动力学,发现通过降低处方中 API 颗粒的粒径,可以显著提高药物释放和经皮吸收,进而提高处方的药效。
分子量:ca.250
logP:1.5
芳香环数:1
TPSA:80Å2
拟开发剂型:水凝胶
溶解度较低:0.28mg/L(水)、30mg/L(溶剂)
拟开发剂量:5-10%(混悬型凝胶)
存在问题:API 颗粒大、溶解速率为吸收速控步骤

释放速率:
2223.4 → 3294.1 μg/(cm2 h0.5) P < 0.001
皮肤吸收:
5.07 → 9.70 μg/cm2 P < 0.001
Noyes-Whitney 方程:
dC/dt=kDA (Cs-Ct) 降低尺寸,增加溶解速率
2
案例
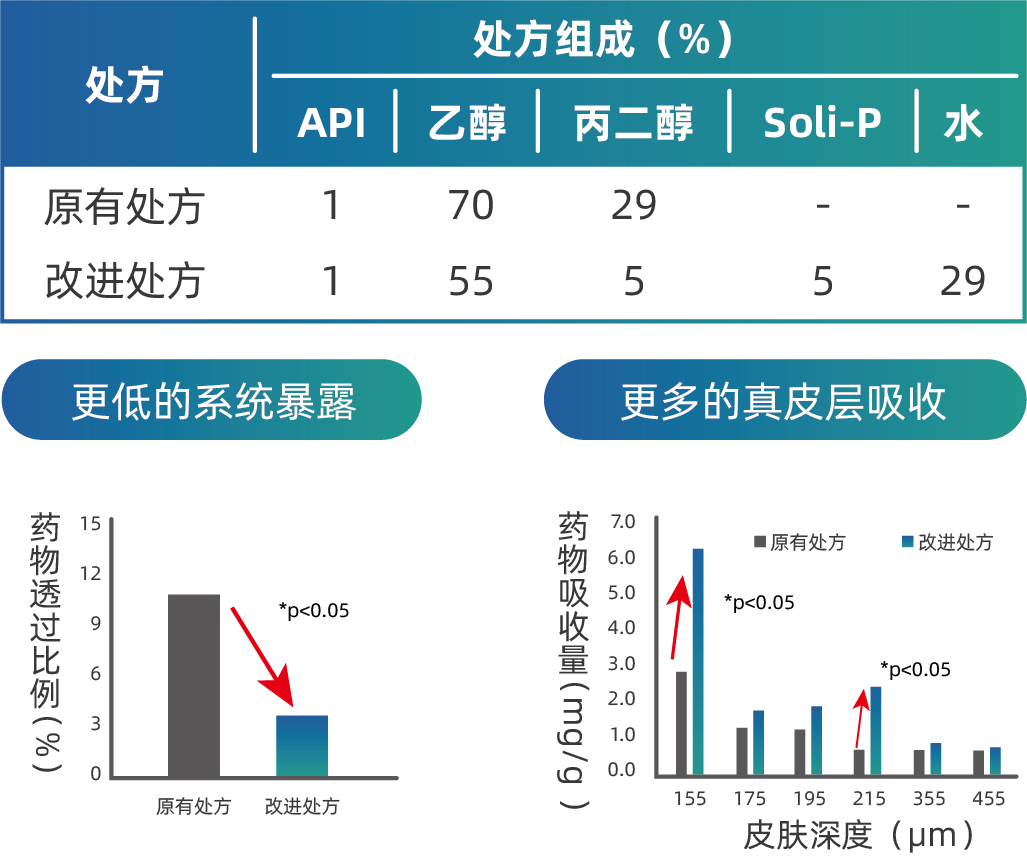
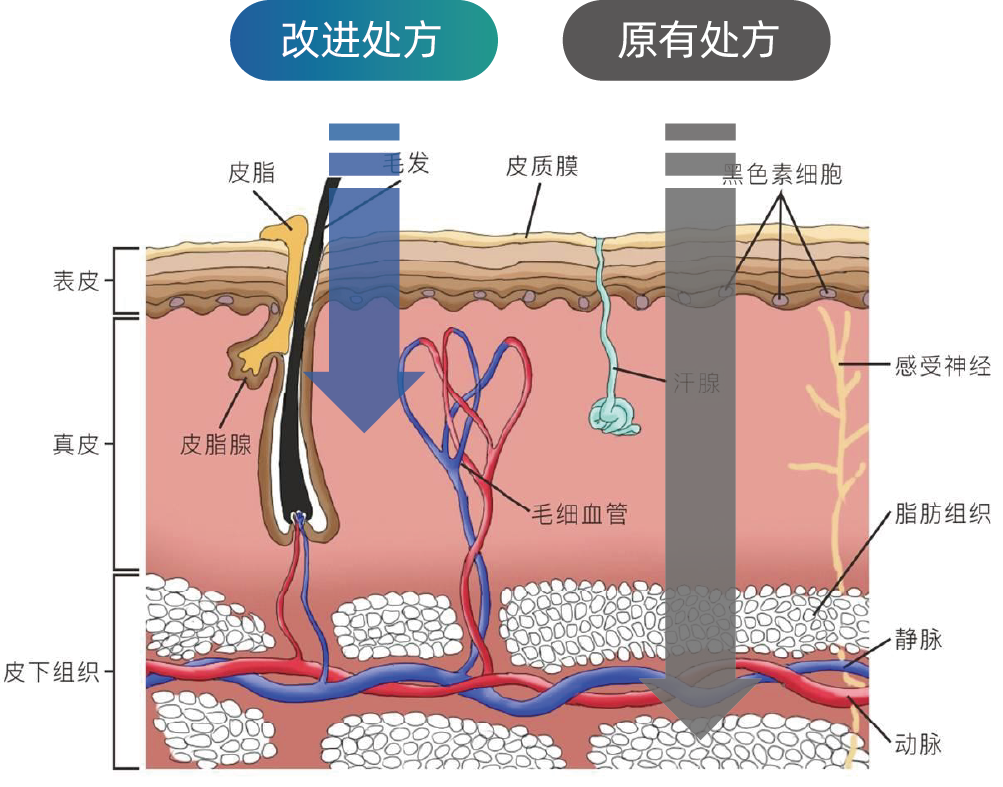
用 IVPT 和皮肤冰冻切片方法研究不同处方的皮肤药代动力学,发现通过改变处方的促渗透剂,既能够显著提高药物在皮肤深层次的吸收(真皮层),又能够显著降低系统暴露量,同时提高了药物的疗效和安全性。
xx溶液剂处方优化:增加药物在真皮层吸收、降低药物系统暴露
3
案例
用 IVPT 和皮肤剥离技术方法研究不同处方的皮肤药代动力学,发现通过纳米晶技术可以显著提高药物在真皮层和毛囊部位药物的吸收,提高了药物的疗效和安全性。


4
案例
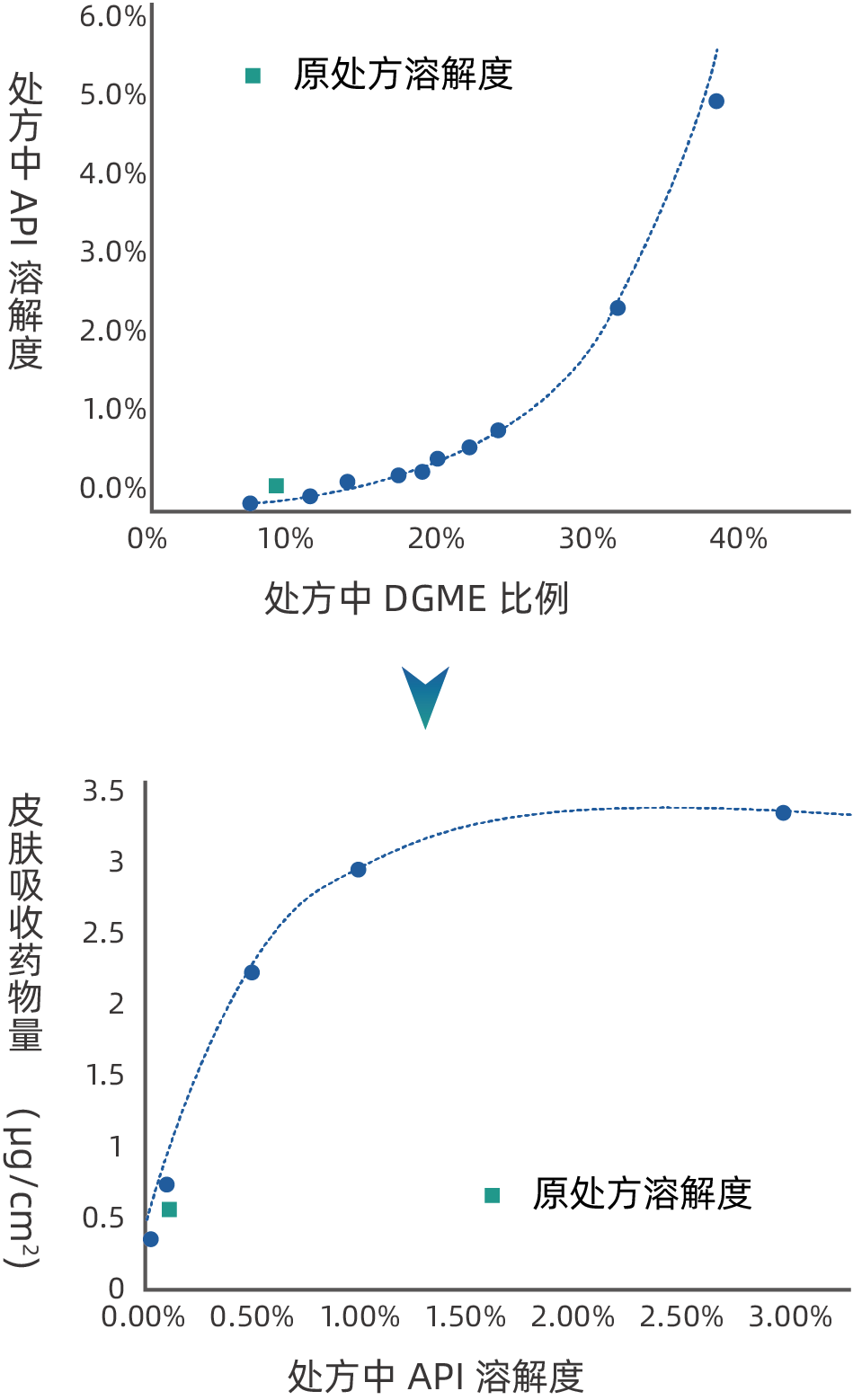
用 IVPT 方法研究不同处方的皮肤药代动力学,发现通过改变处方的溶剂体系,增加处方中API 溶解度,能够显著提高药物的皮肤吸收。

5
案例
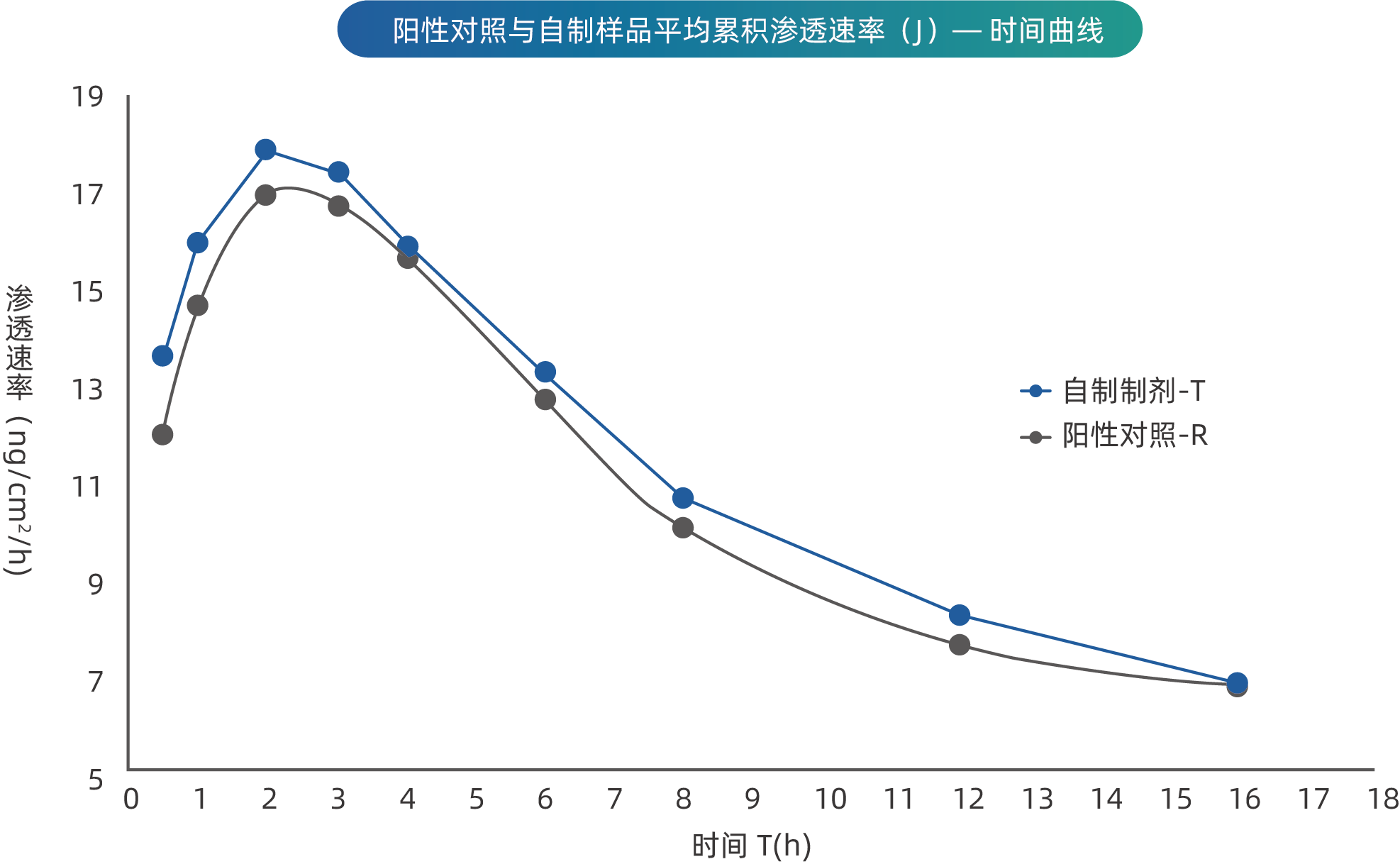
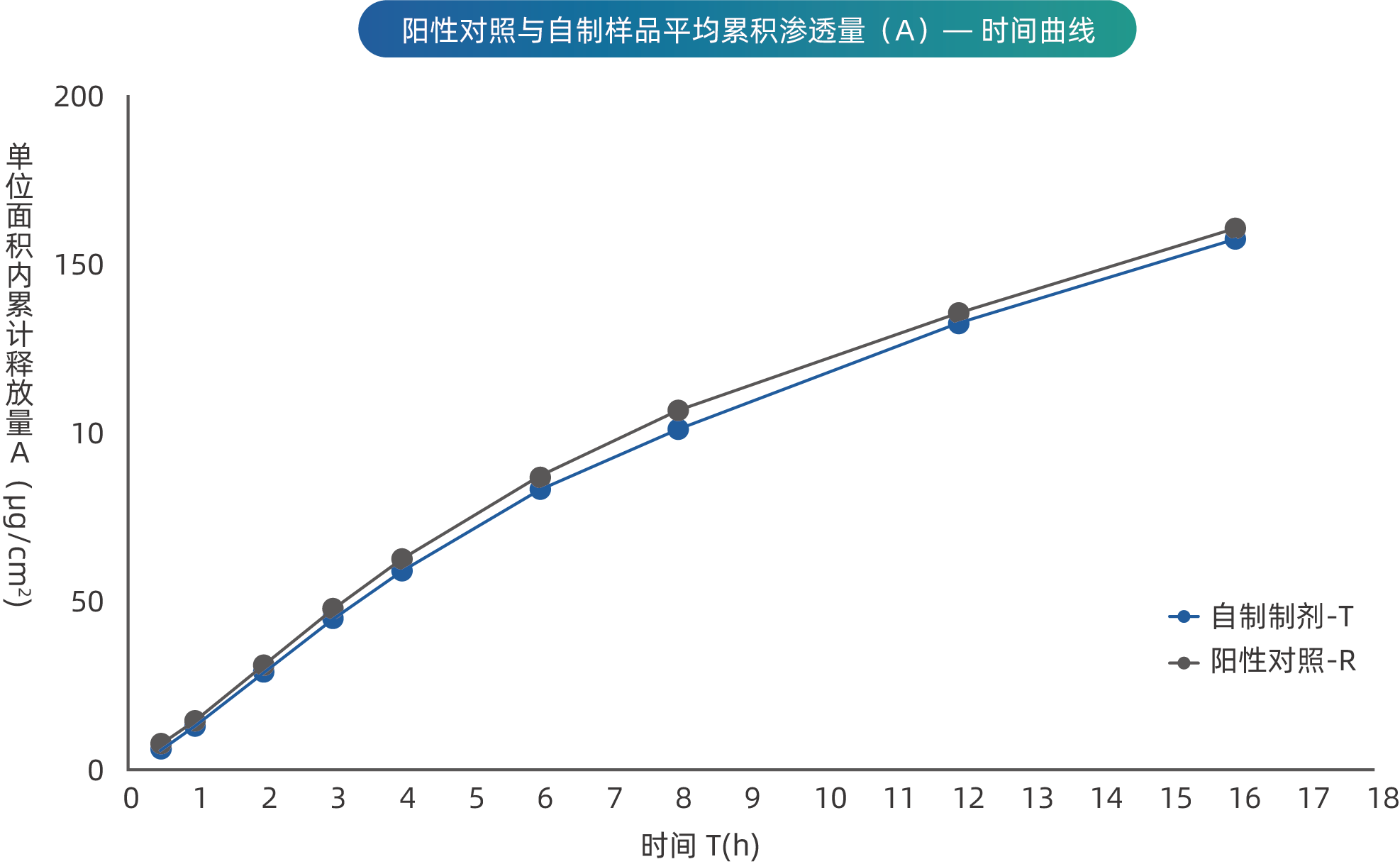
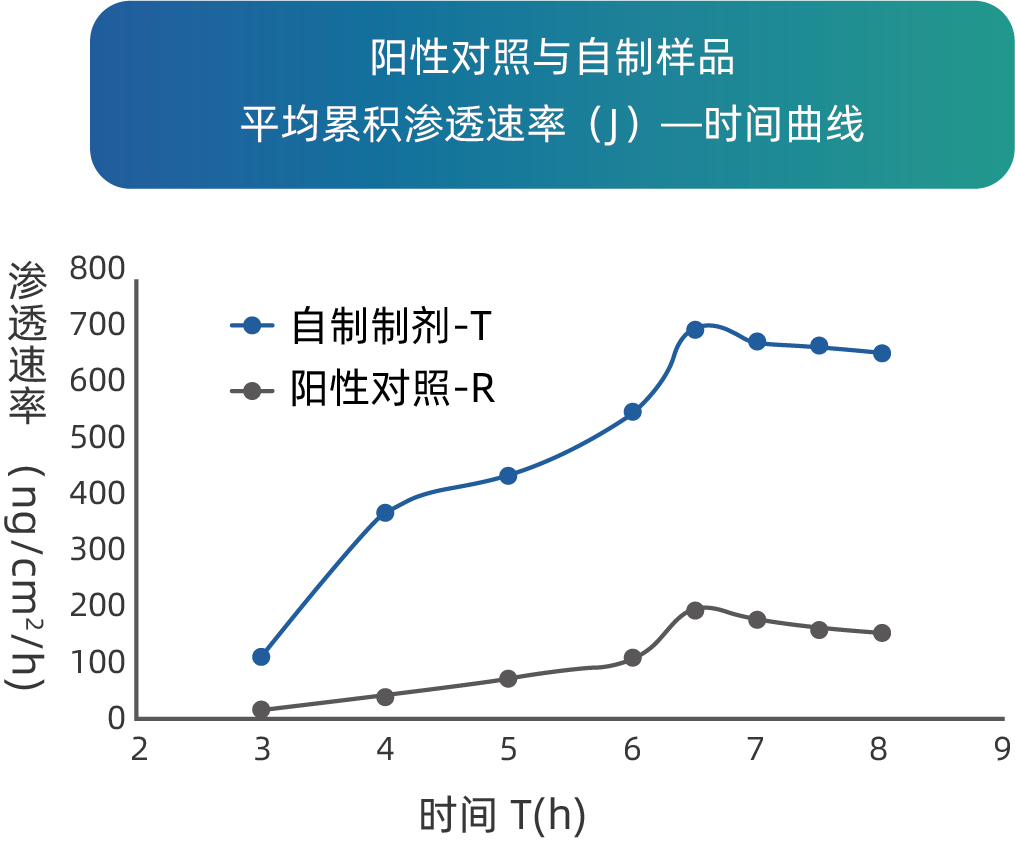
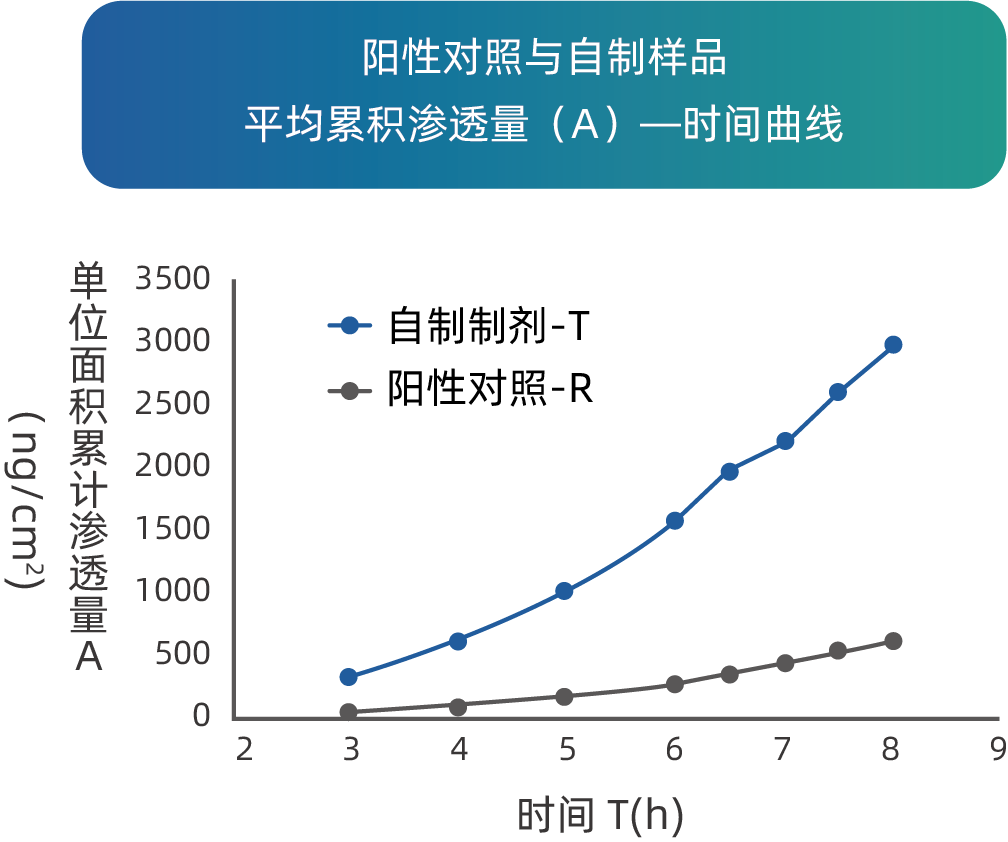
用 IVPT 方法研究不同剂型(T-涂膜剂,R-贴剂)的药物渗透,发现通过涂膜剂技术可以显著提高药物在的皮肤渗透,提高了药物的疗效。
6
其他案例
不同剂型的仿制药的体外释放、体外透皮研究。
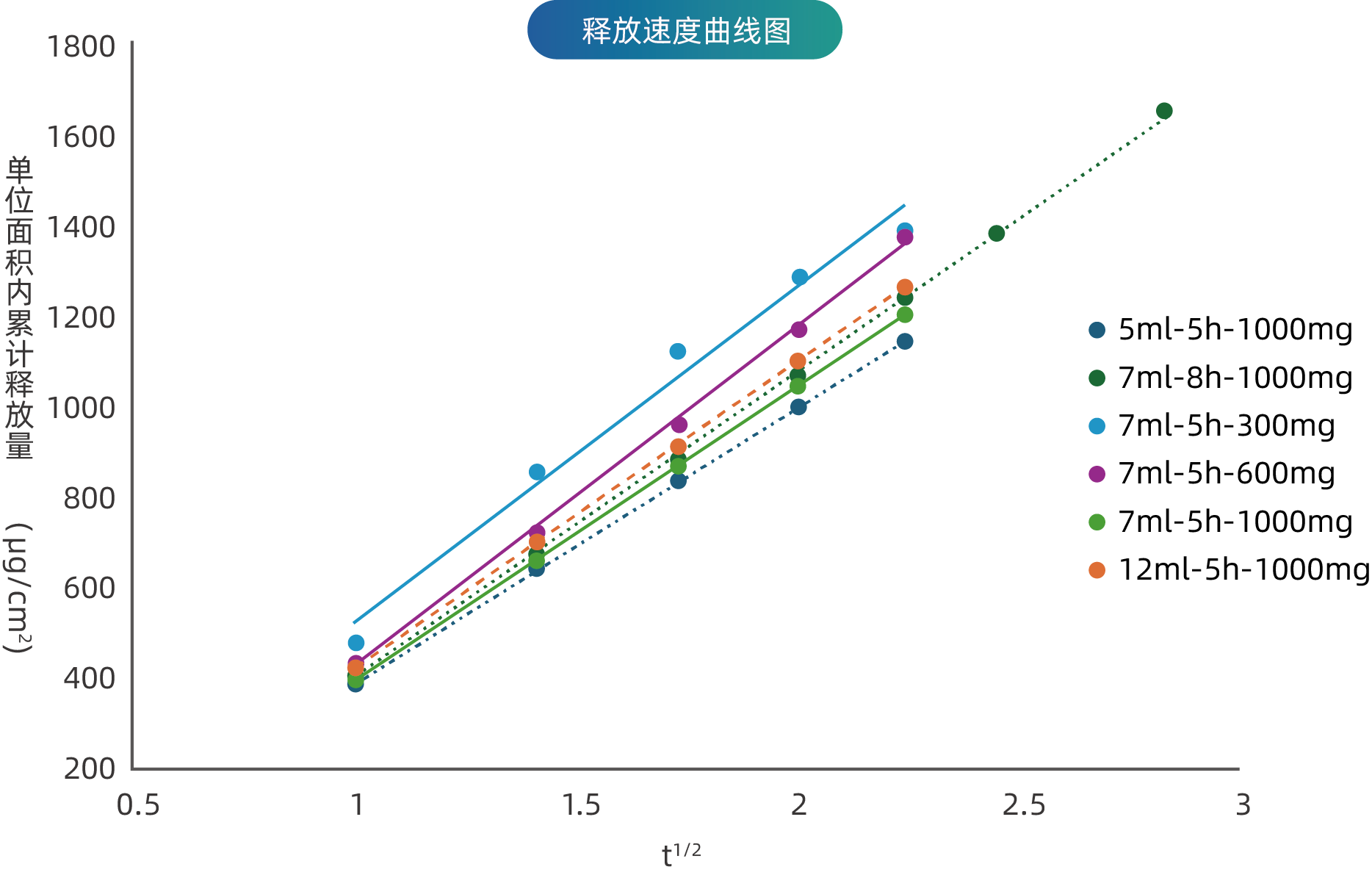
某乳胶剂体外释放:通过对不同介质体积、上样量和取样时间点等全面的试验研究,可快速筛选出合适的方法
某软膏产品仿制药体外透皮试验-IVPT(等效性评价,自研制剂和参比制剂体外渗透曲线及渗透量一致)
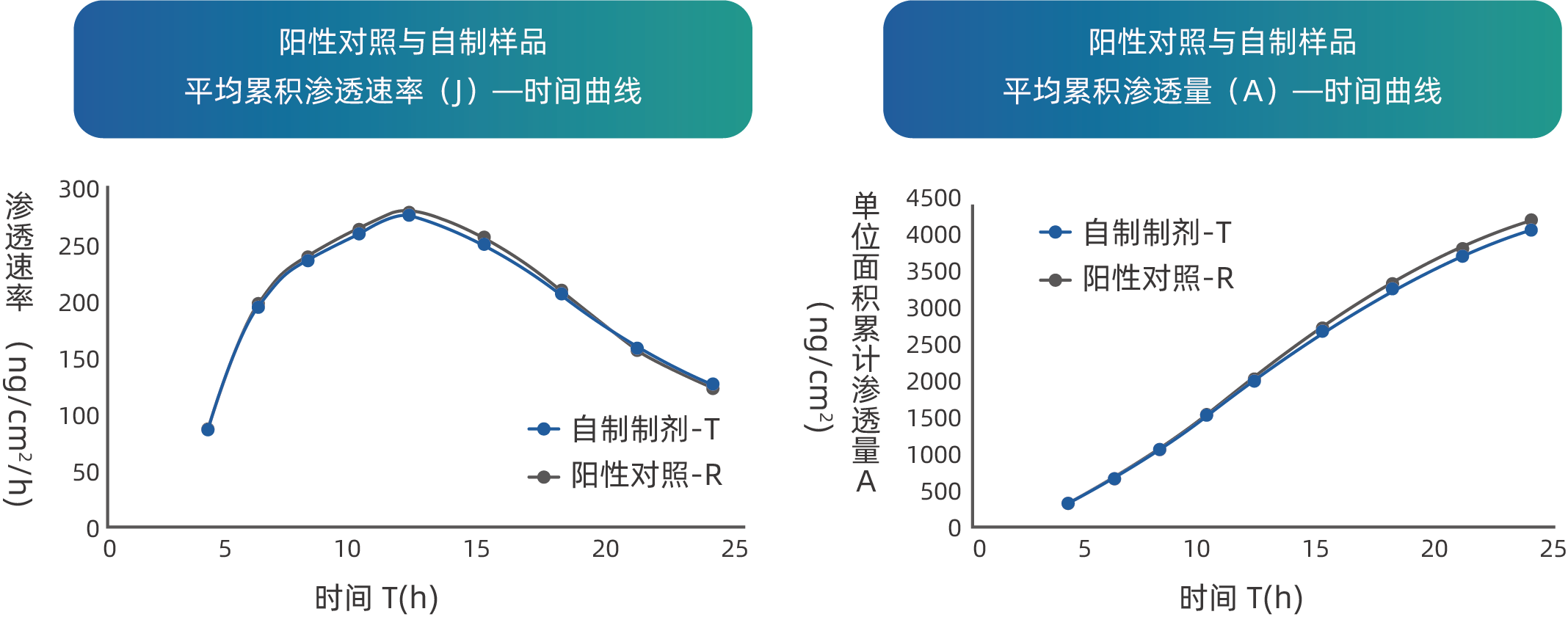
某乳膏产品仿制药体外透皮试验(等效性评价,自研制剂和参比制剂体外渗透曲线及渗透量一致)